§2. Механизм взаимодействия фермента и субстрата. Роль активного центра в ферментативном катализе
Цель изучения этой темы: объяснить механизм образования фермент-субстратного комплекса.
Что такое ферменты? К какому типу веществ они относятся? Какова связь между ферментами и катализаторами; ферментами и ДНК? Какое выражение будет более верным: «Все важнейшие белки – ферменты» или «Все важнейшие ферменты – белки»?

Что нужно повторить для успешного изучения темы? § 5 – учебник для 8 и 10 классов; § 10 – учебник для 9 класса.
Фермент и субстрат. Как вы помните, каталитическая, или ферментативная, функция важна для любых процессов жизнедеятельности, в любой живой клетке. Без молниеносных химических реакций, катализируемых ферментами, жизнь вообще невозможна.
Подавляющее большинство химических реакций, происходящих в живых системах (в клетках или полостях органов), являются каталитическими. В качестве катализаторов выступают строго специфичные белкиферменты.
Среди химиков, специализирующихся на изучении процессов катализа, бытует мнение, что велика вероятность того, что к любой химической реакции, даже не считающейся каталитической, можно подобрать катализатор и сделать реакцию более быстрой или энергетически более выгодной. И также существует мнение, что чуть ли не к любым двум, не способным вступать в химическую реакцию, веществам, можно подобрать некий гипотетический катализатор, что сделает реакцию между ними возможной.
Кроме гипотетических предположений, есть несколько фактов о работе ферментов, считающихся полностью доказанными (рис. 2). Рассмотрим их.
1. Без ферментов и катализируемых ими реакций не обходится ни одна живая система. Даже самые примитивные из бактерий не могут обеспечить свою жизнедеятельность без ферментов.
2. Ферменты четко взаимодействуют с одним субстратом, но иногда встречаются способные реагировать с небольшим количеством химических веществ. То есть существуют ферменты (как и неорганические катализаторы), способные взаимодействовать не только с одним субстратом. В этом случае в зависимости от субстрата может изменяться и продукт катализируемой реакции.
Рис. 2. Работа ферментов
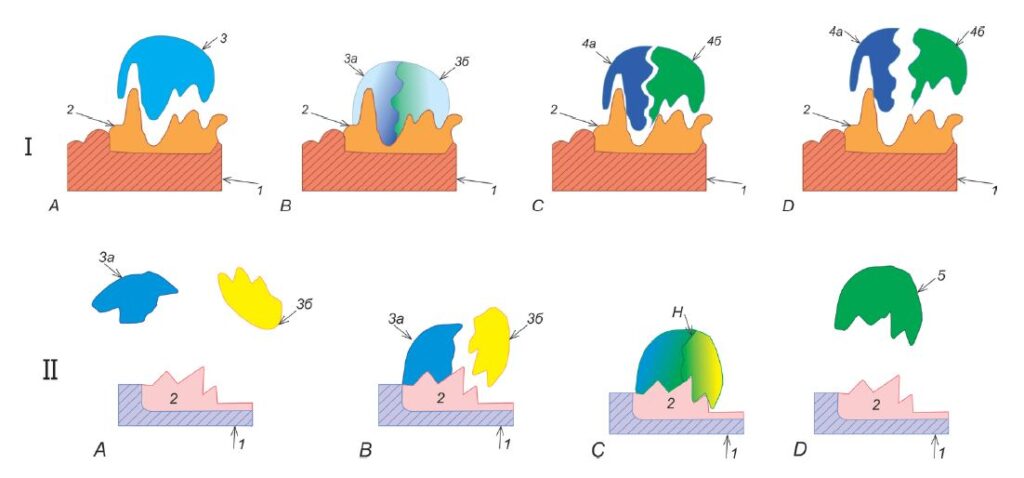
I – ферментативный катализ реакции разложения (например, пищеварительный фермент).
1 – простетическая группа фермента; 2 – активный центр фермента; 3 – субстрат; 3а и 3б – компоненты субстрата, отделяющиеся друг от друга вследствие ферментативной реакции разложения; 4а и 4б – самостоятельные, вновь образовавшиеся вещества – продукт ферментативной реакции разложения. А – фермент и субстрат еще не соединились; В – формирование фермент-субстратного взаимодействия и начало процесса реакции; С – завершение ферментативной реакции разложения – образование продуктов реакции – новых веществ 4а и 4б; D – полное освобождение фермента от продуктов реакции. Теперь он снова готов к взаимодействию с субстратом (A).
II – ферментативный катализ реакции соединения (например, ферменты темновых реакций фотосинтеза).
1 – простетическая группа фермента; 2 – активный центр фермента; 3а – первый субстрат и 3б – второй субстрат – участники реакции соединения; 4 – процесс соединения двух молекул субстратов под воздействием фермента в единое вещество; 5 – вновь образовавшееся вещество – продукт ферментативной реакции соединения.
А – фермент и субстраты еще не взаимодействуют; В – формирование ферментсубстратного комплекса с веществом 3а, соединение вещества 3б с фермент-субстратным комплексом, состоящим из фермента и вещества 3а. Следует помнить, что вещество 3б не способно отдельно взаимодействовать ни с веществом 3а, ни с ферментом; С – сам процесс ферментативной реакции соединения веществ 3а и 3б; D – завершение ферментативной реакции соединения – образование продукта реакции – новое вещество 5, полное освобождение фермента от продуктов реакции. Теперь он снова готов к взаимодействию с субстратами (А).
3. Для активного взаимодействия фермента и субстрата их молекулы должны соприкасаться. То есть вероятность их взаимодействия в растворах или в газообразном состоянии в несколько раз выше и эффективнее, чем в твердом состоянии. Многие ферментативные реакции в сухих веществах вообще не протекают.
4. Если некая химическая реакция может происходить и без фермента, она не является каталитической. В этом случае наличие фермента просто ускоряет реакцию в десятки, сотни и иногда даже тысячи раз. Если же присутствие фермента делает реакцию вообще возможной, тогда она называется каталитической. Иначе говоря, без фермента она вообще не будет протекать (ни при каких иных изменениях физических условий, таких как повышение температуры или увеличение концентрации веществ, поверхности их соприкосновения и т. д.).
5. Ферментативная реакция всегда энергетически более выгодна. За счет фермента растет скорость реакции и (или) падает ее энергоемкость.
Строение молекул фермента. Что же представляет собой молекула фермента? В подавляющем большинстве ферменты – это белки¹. Часто они представляют собой сложные белки, включающие в свой состав, кроме аминокислотных остатков, иные компоненты – простетические группы. Это могут быть ионы металлов, части молекул витаминов (или целые молекулы), иные вещества органической природы (липиды, углеводы, циклические структуры и т. д.). Большая часть молекулы фермента выполняет своего рода вспомогательную роль. Она является механической основой или структурой, на которой размещается его «главная часть». Вот эту самую «главную часть», способную «узнавать» субстрат, и называют активным центром фермента. Чаще всего именно в состав активного центра фермента входят простетические группы.
Роль активного центра в ферментативном катализе заключается в «узнавании» и непосредственном «взаимодействии» с субстратом. Значит, молекула субстрата вступает во взаимодействие не со всеми частями молекулы фермента, а только с ее строго определенной частью – активным центром.
Механизм взаимодействия фермента и субстрата достаточно сложен и изучен не до конца. Но в целом можно представить любой каталитический процесс на следующем гипотетическом примере. Предположим, что реакция соединения между веществами А и В является каталитической. То есть без наличия некоего третьего вещества – катализатора – вещество А вообще не способно химически взаимодействовать с веществом В. Как, например, стекло не вступает в реакцию с водой, как бы мы ни изменяли физические условия.
Если обозначить катализатор (фермент) символом К/Ф, то процесс каталитической реакции соединения веществ А и В можно выразить в следующей схеме-формуле:
А+В+К/Ф→АК/Ф+В=АВ+К/Ф.
Продуктом, т. е. конечным результатом, данной реакции является вещество АВ. Субстратом, взаимодействующим с катализатором-ферментом, является вещество А. Анализируя схему, можно сделать вывод, что вещество А вступает во взаимодействие с катализатором и только после этого получает способность химически взаимодействовать с веществом В. То есть реакция происходит не между веществами А и В. Реакция соединения возможна только (!) между комплексом АК/Ф и веществом В. Результатом – продуктом реакции является новое вещество АВ. При этом по окончании химического процесса целостная молекула неповрежденного фермента К/Ф освобождается из реакции. Именно поэтому в самом упрощенном определении катализатора отмечается, что это «вещества, которые не расходуются в ходе реакций, но делают эти процессы возможными».
Катализатор, фермент, субстрат, продукт, простетическая группа, активный центр фермента, витамины.

Знание и понимание
1. Как вы понимаете, что такое активный центр фермента?
2. Опишите, какие вещества могут входить в простетические группы.
Применение
1. Сравните роль разных частей молекулы фермента.
2. Какие из перечисленных сведений о работе ферментов кажутся вам наиболее важными в практической деятельности? Покажите на конкретных жизненных примерах.
Анализ
1. Изобразите в виде цветной произвольной схемы реакцию разложения крахмала на глюкозу под действием фермента слюны амилазы. Как изменились ваши представления об этом процессе после знакомства с материалом параграфа?
2. Проанализируйте этапы фермент-субстратного взаимодействия.
Синтез
1. Порассуждайте, при химическом изменении каких частей фермента его каталитическая активность может сильно снизиться или вообще исчезнуть, даже если все другие части молекулы не повреждены.
2. Соотнесите свойства и характеристики особенностей функционирования ферментов с функционированием антител и антигенов. Какие сходство и различия вы обнаружили?
Оценка
1. Напишите реферат о применении различных ферментных комплексов при переработке органического сырья (растительного, животного, нефтехимического).
2. Обсудите следующие высказывания и ситуации:
1) В ближайшем будущем ученые откроют катализаторы для химических реакций между всеми веществами на Земле.
2) Что произойдет, если биологически активный фермент, например лизоцим слюны, довести до 60 градусов? Предположите, как это отразится на его активности. Произойдут ли изменения активности, если после нагревания его остудить?
¹ Ферменты небелковой (и даже неорганической) природы обнаружены в живых системах. Как правило, их в сотни и тысячи раз меньше. Поэтому мы не будем рассматривать их в данном школьном курсе.